Віч етіологія епідеміологія патогенез. ВІЛ-інфекція (HIV infection). Епідеміологія. Клінічна картина. Профілактика. ? До групи ризику інфікування ВІЛ належать
Ризик ВІЛ-інфікування при незахищеному сексі у жінок приблизно в 8 разів вищий, ніж у чоловіків. У жінок у ранній фазі ВІЛ-інфекції більш виражена імунна активація, що призводить до менш вираженої реплікації вірусу, проте надалі, при хронізації процесу, цей механізм забезпечує більш високу швидкість прогресування захворювання. На тлі АРТ у жінок відбувається менш виражене зниження рівня маркерів запалення, ніж чоловіки. Жінки частіше, ніж чоловіки, переривають АРТ, зокрема самостійно. У той же час, заміжні жінки, які перебувають у шлюбі з віковим партнером, мають максимальну відданість лікуванню. У жінок частіше, ніж у чоловіків, виникають побічні ефектиАРТ.
ВІЛ-інфекція та планування вагітності
Вагітність при ВІЛ-інфекції можлива, тому що ризик передачі ВІЛ-інфекції своєму сексуальному партнеру, а також дитині сьогодні може бути значною мірою знижений, а часом навіть повністю виключений. ВІЛ-інфіковані особи не передають ВІЛ за сексуальних контактів за таких умов:
- ВІЛ-інфікований пацієнт отримує АРТ під контролем лікаря;
- вірусне навантаження зберігається на невизначеному рівні протягом щонайменше 6 місяців;
- відсутні інші інфекції, що передаються статевим шляхом.
ВІЛ-інфекція у дітей
Переважна більшість випадків діти інфікуються від матері вертикальним шляхом. Горизонтальний шлях передачі інфекції: гемотрансфузії, сексуальні контакти, вживання наркотиків для дітей практично виключено. Типові для дорослих ознаки гострої ВІЛ-інфекції, такі як лихоманка, біль у горлі та лімфаденопатія, у дітей не спостерігаються. У той самий час наявність антитіл до ВІЛ у крові який завжди підтверджує наявність інфекції. Оскільки у грудному віці ризик смерті від СНІДу надзвичайно високий, починати АРТ необхідно у перші 12 місяців життя, незалежно від вірусологічних, імунологічних та клінічних критеріїв.
Терапія при ВІЛ/СНІД
В даний час ВІЛ-інфекція піддається лікуванню препаратами АРТ. Хоча повне одужання поки що неможливе, але є можливість хворобу контролювати. Метою АРТ є продовження життя та покращення його якості у хворих на ВІЛ-інфекцію, запобігання розвитку СНІД.
Завдання АРТ:
- клінічні: попередження розвитку опортуністичних інфекцій та ВІЛ-асоційованих неінфекційних захворювань;
- вірусологічні: максимальне та тривале пригнічення реплікації ВІЛ;
- імунологічні: відновлення та підтримання функції імунної системи;
- епідеміологічні: зменшення кількості випадків передачі ВІЛ
Якомога раніше ранній початок АРТ може мати довгострокові імунологічні і вірусологічні переваги для інфікованого, а й запобігти розвитку резистентності при непоміченої інфекції під час передекспозиційної профілактики.
АРТ призначається:
- всім пацієнтам із кількістю лімфоцитів CD4+< 500 мкл -1 независимо от стадии заболевания. Пациентам с количеством лимфоцитов CD4+ >500 мкл -1 АРТ може бути призначений при готовності приймати терапію довічно. Рекомендується призначати АРТ незалежно від кількості CD4+ лімфоцитів при їх швидкому зниженні (> 100 мкл -1 на рік);
- всім пацієнтам незалежно від кількості лімфоцитів CD4+ за наявності клінічних проявів вторинних захворювань, особливо у разі розвитку СНІД-індикаторних захворювань, а в деяких випадках АРТ може бути відкладена для запобігання розвитку запального синдрому відновлення імунної системи;
- при гострій ВІЛ-інфекції довічно;
- всім пацієнтам незалежно від кількості лімфоцитів CD4+ та стадії захворювання у наступних ситуаціях:
- пацієнтам із активною формою туберкульозу;
- гепатитом В, якщо показано його лікування, або за наявності ознак тяжкого хронічного ураження печінки;
- пацієнтам із супутнім хронічним гепатитом С (при кількості лімфоцитів CD4+ > 500 мкл АРТ може бути відкладена до завершення курсу його лікування;
- пацієнтам із ВІЛ-асоційованою нефропатією;
- пацієнтам із захворюваннями, що вимагають тривалого застосування терапії, що пригнічує імунітет (променева терапія, кортикостероїдні гормони, цитостатики);
- вагітним;
- тромбоцитопенія;
- пацієнтам старше 60 років з ВІЛ-асоційованими нейрокогнітивними розладами;
- при вірусному навантаженні > 100 000 копій/мл плазми;
- за епідеміологічними показаннями: інфікований ВІЛ-партнер у дискордантній парі, при підготовці ВІЛ-інфікованого пацієнта до застосування допоміжних репродуктивних технологій.
При проведенні АРТ не допускається її переривання, інакше відбувається рецидив інфекції та розвиток резистентності збудника.
Профілактика ВІЛ-інфекції
Профілактика ВІЛ-інфекції включає:
- виключення безладних статевих зв'язків;
- сексуальний зв'язок із надійним партнером;
- використання засобів запобігання при випадкових статевих контактах;
- виключення вживання будь-якої форми наркотичних засобів;
- проведення процедур пірсингу, татуювання, проколювання вух у спеціальних закладах;
- використання індивідуальних предметів особистої гігієни
Постконтактна профілактика ВІЛ-інфекції
Постконтактна профілактика є короткостроковим курсом АРТ для зниження ймовірності розвитку захворювання після контакту з біологічними субстанціями, інфікованими ВІЛ. Біологічні субстанції, при контакті з якими можливе зараження ВІЛ:
- кров;
- сперма;
- вагінальні виділення;
- синовіальна рідина;
- спинномозкова рідина;
- плевральна рідина;
- перикардіальна рідина;
- амніотична рідина;
- будь-які рідини з домішкою крові;
- що містять ВІЛ-культури та культуральні середовища.
Крім того, існує низка непередбачених (аварійних) ситуацій, які можуть призвести до зараження ВІЛ:
- контакт із кров'ю або біологічними субстанціями, що контаміновані ВІЛ, при виконанні професійних обов'язків медичним персоналом;
- незахищений статевий контакт із ВІЛ-інфікованим, використання нестерильних шприців, випадкові уколи голками тощо).
У разі виникнення аварійної ситуації на робочому місці медичний працівникзобов'язаний негайно провести комплекс заходів щодо запобігання зараженню ВІЛ-інфекцією:
- у разі порізів та уколів негайно зняти рукавички, вимити руки з милом під проточною водою, обробити руки 70% розчином етилового спирту, змастити ранку 5% спиртовим розчином йоду;
- при попаданні крові або інших біологічних рідин хворого на шкірні покриви це місце обробляють 70% розчином етилового спирту, обмивають водою з милом та повторно обробляють 70% розчином етилового спирту;
- при попаданні крові та інших біологічних рідин хворого на слизову оболонку очей, носа і рота ротову порожнину промивають великою кількістю води і прополіскують 70% розчином етилового спирту, слизову оболонку носа та очей рясно промивають водою (не терти);
- при попаданні крові та інших біологічних рідин хворого на халат, одяг знімають робочий одяг і занурюють його в дезінфікуючий розчин або в бікс для автоклавування.
Застосування АРТ слід розпочати протягом перших двох годин після аварії, але не пізніше 72 годин. Медикаментозна профілактика повинна проводитись під контролем фахівців регіональних центрів профілактики та боротьби зі СНІД, які оцінюють рівень ризику інфікування ВІЛ та призначають необхідну схему АРТ.
Тривалість життя хворих на ВІЛ-інфекцію
Відома мінімальна тривалість життя становить близько 3-х місяців. Середня – протягом 13 років гине кожен другий пацієнт. Відома максимальна тривалість життя становить понад 20 років.
Консультація спеціаліста регіонального Центру профілактики та боротьби зі СНІДом.
Глава 19. ВІЛ-ІНФЕКЦІЯ
Глава 19. ВІЛ-ІНФЕКЦІЯ
ВІЛ-інфекція - хронічне прогресуюче захворювання людини, що викликається ретровірусом, при якому уражається імунна система та формується імунодефіцитний стан, що призводить до розвитку опортуністичних та вторинних інфекцій, а також злоякісних пухлин.
19.1. етіологія
Збудник даного захворювання виділений у 1983 р. та названий вірусом імунодефіциту людини – ВІЛ (Human Immunodeficiency Virus – HIV).Вірус відноситься до сімейства ретровірусів.
В даний час відомі 2 штами вірусу імунодефіциту людини: ВІЛ-1 та ВІЛ-2.
Вірусна частка має розмір близько 100 нм і є ядро, оточене оболонкою. Ядро містить РНК та особливий фермент (зворотну транскриптазу, або ревертазу), завдяки якому генетичний матеріал вірусу вбудовується в ДНК клітини-господаря, що призводить до подальшого розмноження вірусу та загибелі клітин. У складі оболонки вірусної частки міститься глікопротеїд gp120, який обумовлює тропізм вірусу до клітин організму людини, що має CD4+-рецептори.
Як усі ретровіруси, ВІЛ нестійкий у зовнішньому середовищі, повністю інактивується нагріванням при температурі 56 °С протягом 30 хв, гине при кип'ятінні або зміні реакції середовища (pH нижче 0,1 і вище 13), а також при впливі традиційних дезінфікуючих засобів ( розчини 3-5% хлораміну, 3% хлорного вапна, 5% лізолу, 70% етилового спирту тощо). У біологічних рідинах (кров, сперма) вірус може довго зберігатися у висушеному чи замороженому стані.
19.2. Епідеміологія
Інкубаційний період продовжується близько 1 міс.
Джерелом зараження служить ВІЛ-інфікована людина як у стадії безсимптомного носійства, так і при розгорнутих клінічних проявах захворювання.
У найбільшій кількості вірус виявлений у крові, спермі, спинномозковій рідині, грудному молоці, піхвовому та цервікальному секретах, а також у біоптатах різних тканин. У невеликій кількості, недостатній для інфікування, виявляється у слині, слізній рідині, сечі.
Шляхи передачі ВІЛ: контактно-статевий та парентеральний.
Контактно-статевий шлях передачі характеризується проникненням вірусу в організм через пошкоджену шкіру і слизові оболонки (які рясно кровопостачаються і мають високу всмоктувальну здатність). Неуражений епідерміс практично непроникний для вірусних частинок.
Статевий шлях передачі спостерігають при статевих контактах (гетеро- та гомосексуальних) і пов'язаний, мабуть, з мікротравмами слизових оболонок, що особливо велике при аногенітальних та орогенітальних контактах, а також за наявності запальних захворювань статевих органів.
Парентеральний шлях передачі характеризується попаданням вірусу безпосередньо в кровоносне русло і зустрічається при гемотрансфузіях зараженої крові або її компонентів, ін'єкціях із використанням забруднених інструментів, особливо при застосуванні наркотиків, трансплантаціях органів та тканин донорів.
Інфікування дитини найчастіше відбувається трансплацентарнопід час вагітності чи під час пологів. Відзначено, що у дітей, народжених ВІЛ-інфікованими матерями, захворювання розвивається лише у 25-40% випадків, що пов'язано зі станом матері та акушерськими втручаннями. Так, висока концентрація вірусу в крові або СНІД у матері, недоношеність дитини, природні пологи та контакт дитини з материнською кров'ю підвищують ризик передачі ВІЛ, але жоден із цих факторів не дозволяє передбачити ймовірність зараження дитини. Зараження дитини може статися також при годівліВІЛ-інфікованої матері грудьми,а також зцідженимгрудним молоком.
Групи ризику(Найчастіше інфіковані особи): наркомани, гомосексуалісти та бісексуали, повії, а також особи, схильні до частої зміни статевих партнерів.
19.3. ПАТОГЕНЕЗ
Проникнувши в організм, вірус за допомогою глікопротеїду gp120 фіксується на мембрані клітин, що мають СD4+-рецептори. Дані рецептори розташовуються переважно на Т-хелперах лімфоцитів, які відіграють основну роль розвитку імунної відповіді, а також на моноцитах, макрофагах і деяких інших клітинах. З поверхні клітин проникає вглиб РНК вірусу, трансформується за допомогою ферменту зворотної транскриптази в ДНК клітини, та синтезуються нові вірусні частки, що призводить до загибелі Т-лімфоцитів. Заражені моноцити, на відміну лімфоцитів, не гинуть, а служать резервуаромлатентної інфекції
При ВІЛ-інфекції в організмі порушується співвідношення Т-хелперів та Т-супресорів. Поразка Т-хелперів тягне за собою зниження активності макрофагів і натуральних кілерів, зменшується продукція антитіл В-лімфоцитами, що в результаті призводить до вираженого ослаблення імунної відповіді.
Результатом імунодефіцитного стану стає розвиток різних опортуністичних інфекцій, вторинного інфікування, злоякісних новоутворень.
19.4. КЛАСИФІКАЦІЯ ВІЛ-ІНФЕКЦІЇ
Відповідно до класифікації В.І. Покровського, з 1989 р., виділяють 5 стадій ВІЛ-інфекції.
Інкубаційний період
Інкубаційний період становить 2-8 тижнів. Клінічні прояви відсутні, але ВІЛ-інфікована людина може бути джерелом зараження. Антитіла до вірусу ще не визначаються.
Первинно-маніфестний (гострий) період
У 50% хворих захворювання починається з неспецифічних клінічних проявів: лихоманки, міалгій та артралгій, лімфоаденопатій, нудоти, блювання, діареї, шкірних висипань тощо.
У деяких хворих цей період хвороби протікає безсимптомно.
Вірус у крові визначається за допомогою ПЛР. Антитіла до ВІЛ можуть не виявлятися.
Латентний період
Латентний період триває кілька років (від 1 до 8-10 років). Клінічні прояви відсутні, імунний статус не змінюється, але людина є джерелом інфекції (наголошується на вірусоносій). Виявляють антитіла до ВІЛ за допомогою методу ІФАта реакції імуноблотінгу.
Наприкінці латентного періоду розвивається генералізована лімфаденопатія. Діагностичне значення має збільшення (більше 1 см) двох лімфатичних вузлів і більше (крім пахових) у не пов'язаних один з одним областях тривалістю понад 3 місяці.
СНІД (стадія вторинних захворювань)
Основні клінічні прояви СНІДу - лихоманка, нічна пітливість, швидка стомлюваність, втрата маси тіла (до кахексії), діарея, генералізована лімфаденопатія, гепатоспленомегалія, пневмоцистна пневмонія, прогресуючі неврологічні порушення, кандидозу.
Термінальна стадія
Наростають кахексія, загальна інтоксикація, деменція, прогресують інтеркурентні захворювання. Закінчується процес летальним результатом.
19.5. ШКІРНІ ПРОЯВИ ПРИ СНІДУ
Відмінні риси шкірних захворювань при СНІДі - тривалий рецидивуючий перебіг, поширений характер висипань, нетипова локалізація, невластивий віковий період, слабка ефективність звичайної терапії.
Мікози
Розвиток грибкових захворювань у ВІЛ-інфікованих пацієнтів – ранній клінічний симптом імунодефіцитного стану.
Кандидоз шкіри та слизових оболонок
Кандидоз шкіри та слизових оболонок виникає практично у всіх хворих на СНІД. Найчастіше виявляється кандидозом слизових оболонок порожнини рота, хейлітом, езофагітом, кандидозом великих складок (дріжджові попрілості), ураженням аногенітальної області, кандидозом зовнішнього слухового проходу, ураженням нігтьових валиків (кандидозна пароніхія), нігтьових пластин.
Особливості перебігу кандидозу при СНІДі - ураження осіб молодого віку, особливо чоловіків, тенденція до утворення великих вогнищ ураження, схильність до ерозування та виразки.
Руброфітія
Руброфітія - часта форма мікозу гладкої шкіри у хворих на СНІД. Протягом захворювання привертають увагу поширеність висипань, поява інфільтрованих елементів, а при мікроскопічному дослідженні - велика кількість міцелію.
Себорейний дерматит та різнобарвний лишай
Себорейний дерматит та різнобарвний лишай - захворювання, що відносяться до групи малацезіозів та викликані дріжджоподібною ліпофільною флорою Malassezia furfur.
Себорейний дерматит
Себорейний дерматит виявляють більш ніж у половини ВІЛ-інфікованих вже у ранньому періоді. Зазвичай захворювання починається з себорейних зон (обличчя, волосиста частина голови, вушні раковини тощо), а надалі поширюється на шкіру тулуба, верхні та нижні кінцівки (аж до еритродермії). Висипання супроводжуються рясним лущенням, формуванням кірок, у складках виникають ерозії, випадає волосся.
Різнокольоровий лишай
Різнобарвний лишай у ВІЛ-інфікованих характеризується появою на шкірі великих інфільтрованих плям, що трансформуються у бляшки.
Вірусні захворювання шкіри
Простий герпес
Простий герпес – типове захворювання у ВІЛ-інфікованих пацієнтів та протікає з частими рецидивами, майже без ремісій. Відрізняється великою кількістю елементів, аж до дисемінованого ураження, а також схильністю до ерозування і виразки, що супроводжується вираженою хворобливістю. Нерідко місцях висипань формуються рубці. При повторному застосуванні ацикловіру швидко розвивається резистентність до цього препарату.
Оперезуючий герпес
Оперезуючий герпес на тлі ВІЛ-інфекції набуває рецидивуючого перебігу, що дуже рідко зустрічається у пацієнтів молодого віку і є раннім маркером імуносупресивного стану. Рецидивуючу форму оперізувального герпесу в осіб до 60 років у даний час розглядають як один з ВІЧіндикаторних захворювань (особливо за наявності у пацієнтів стійкої лімфаденопатії).
Клінічно захворювання характеризується поширеністю, частим розвитком гангренозних (некротичних) форм, вираженою хворобливістю, тривалими невралгіями, формуванням рубців.
Контагіозний молюск
Контагіозний молюск - вірусне захворювання, більш характерне для молодшого дитячого віку, дуже поширене серед ВІЛ-інфікованих пацієнтів, у яких набуває дисемінованого рецидивуючого характеру. Найчастіша локалізація висипань - обличчя, шия, волосиста частина голови, де елементи стають великими (більше 1 см), зливними.
Волосата лейкоплакія порожнини рота
Волосата лейкоплакія порожнини рота - захворювання, описане тільки у ВІЛ-інфікованих хворих, викликається вірусом Епштейна-Барр та папіломавірусом. Клінічно є потовщенням
слизової оболонки латеральної поверхні язика у вигляді бляшки білястого кольору, покритої тонкими кератотичними волосками, довжина яких становить кілька міліметрів.
Бородавки
Бородавки викликаються різними типами вірусу папіломи людини. У ВІЛ-інфікованих пацієнтів частіше, ніж у популяції, виявляють поширені форми вульгарних, долонно-підошовних та аногенітальних (гострі кондиломи) бородавок.
Піодермії
Піодермії часто зустрічаються у хворих на СНІД. Характеризуються важким перебігом і часто призводять до розвитку сепсису. Найбільш типово розвиток фолікулітів, фурункульозу, ектими, рупіоїдної піодермії, хронічної дифузної стрептодермії, виразково-гетируючої піодермії та інших форм. У ряді випадків спостерігають атипові піодермії, які викликаються грамнегативною флорою.
Короста
Короста на фоні імунодефіцитного стану протікає дуже важко - у вигляді норвезької корости, яка характеризується високою контагіозністю для оточуючих, а клінічно - повсюдною локалізацією висипів, масивними корковими нашаруваннями, порушенням загального стану.
Пухлини шкіри
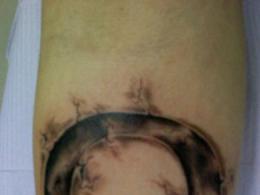
Саркома Капоші – злоякісна пухлина кровоносних судин – достовірний клінічний прояв ВІЛ-інфекції. Захворювання розглядають як СНІД-індикаторне захворювання. Характеризується появою на шкірі, слизових оболонках, внутрішніх органах судинних вузликів темно-вишневого чи чорного кольору. На відміну від класичного типу саркоми Капоші (який зустрічається у пацієнтів старечого віку, характеризується повільним розвитком клінічної картини, рідкісним залученням до процесу внутрішніх органів та типовою початковою локалізацією на стопах та гомілках), СНІД-асоційована саркома Капоші віку, характеризується злоякісним перебігом з мета-
стазуванням пухлини у внутрішні органи (легкі, кістки, головний мозок тощо), а первинні висипання можуть з'являтися не тільки на гомілках, а й на обличчі, волосистій частині голови, вушних раковинах, слизовій оболонці ротової порожнини (рис. 19- 1, 19-2).
Лікарська токсикодермія
Лікарська токсикодермія у ВІЛ-інфікованих зазвичай розвивається на фоні терапії котримоксазолом і протікає за кореподібним типом. Ця реакція розвивається у 70% хворих.
Рис. 19-1.Саркома Капоші на стопі

Рис. 19-2.Саркома Капоші на гомілки
19.6. ОСОБЛИВОСТІ ПЕРЕЧЕННЯ ВІЛ-ІНФЕКЦІЇ У ДІТЕЙ
Зараження дітей відбувається переважно вертикальним шляхом передачі (від ВІЛ-інфікованої матері дитині): внутрішньоутробно, під час пологів або при годівлі грудьми.
Діти, народжені від ВІЛ-інфікованих матерів, хворіють на 25-40% випадків. При народженні дітей від серопозитивних матерів вирішення питання про наявність ВІЛ-інфекції у дитини може бути утруднено, оскільки зазвичай новонароджені серопозитивні (материнські антитіла в крові дитини зберігаються до 18 місяців), незалежно від того, чи вони інфіковані чи ні. У дітей молодше півтора року життя діагноз ВІЛ підтверджують виявленням вірусних нуклеїнових кислот методом ПЛР.
Перші клінічні прояви ВІЛ-інфекції у дитини при перинатальному зараженні виникають раніше 4-месячного віку. У більшості дітей безсимптомний період триває довше – у середньому близько 5 років.
Найбільш типові ураження шкіри у дітей – кандидоз слизової оболонки порожнини рота та стравоходу, себорейний дерматит, а також стафілодермії, герпетичні гінгівостоматити, поширений гігантський контагіозний молюсок, оніхомікози. У дітей нерідко виникає геморагічний висип (петехіальний або пурпурозний), що розвивається на тлі тромбоцитопенії.
Саркома Капоші та інші злоякісні новоутворення не є характерними для дитячого віку.
19.7. ЛАБОРАТОРНІ ДОСЛІДЖЕННЯ
Методи, що визначають наявність антитіл до ВІЛ
Відбірковий метод - імуноферментний метод (ІФА), при якому через 3 місяці після зараження визначаються антитіла до ВІЛ у 90-95% хворих. У термінальній стадії кількість антитіл може знижуватися до повного зникнення.
Для підтвердження даних ІФА застосовують метод імуноблот,при якому виявляють антитіла до певним білкам вірусу.Даний метод рідко дає хибнопозитивні результати.
Методи, що визначають наявність вірусних часток у крові
Метод ПЛР дозволяє визначити кількість копій РНК ВІЛ за 1 мкл плазми крові. Наявність будь-якого числа вірусних частинок у сиво-
роті крові доводить ВІЛ-інфікованість. Даний метод також застосовують визначення ефективності противірусного лікування.
Методи, що дозволяють оцінити стан імунітету
Визначають кількість T-хелперів (CD4) та T-супресорів (CD8), а також їх співвідношення. У нормі Т-хелпери становлять понад 500 клітин мкл, а коефіцієнт CD4/CD8 становить 1,8-2,1. При ВІЛ-інфекції кількість Т-хелперів значно знижується та визначається співвідношення менше 1.
19.8. ДІАГНОСТИКА
Діагностика ґрунтується на характерних скаргах (втрата маси тіла, підвищена стомлюваність, кашель, діарея, тривала лихоманка і т.д.), клінічній картині (виявлення стигм наркоманії, лімфаденопатії, наявність СНІД-асоційованих дерматозів та інших інфекційних інфекцій) даних лабораторних досліджень.
19.9. ЛІКУВАННЯ
Для лікування ВІЛ-інфекції застосовують 3 класи антиретровірусних препаратів.
Нуклеозидні інгібітори зворотної транскриптази (зидовудін по 200 мг внутрішньо 4 рази на день, для дітей дозу розраховують виходячи з 90-180 мг/м 2 внутрішньо 3-4 рази на день; диданозин по 200 мг внутрішньо
2 рази на день, для дітей – 120 мг/м 2 внутрішньо 2 рази на день; а також стравудин, ламівудін та ін.
Ненуклеозидні інгібітори зворотної транскриптази (залцитабін 0,75 мг внутрішньо 3 рази на день, для дітей – по 0,01 мг/кг внутрішньо
3 рази на день; абакавір по 300 мг внутрішньо 2 рази на день, для дітей - 8 мг/кг внутрішньо 2 рази на день.
Інгібітори протеаз ВІЛ (нелфінавір по 750 мг внутрішньо 3 рази на день, для дітей – по 20-30 мг/кг 3 рази на день; ритонавір по 600 мг 2 рази на день, для дітей – по 400 мг/м 2 внутрішньо 2 рази на день, а також саквінавір, ампренавір та ін.
Найбільш ефективні схеми лікування, які включають 2 нуклеозидні інгібітори зворотної транскриптази в поєднанні з інгібітором.
протеази або з ненуклеозидним інгібітором зворотної транскриптази.
ВІЛ-інфікованим пацієнтам проводять терапію злоякісних пухлин та опортуністичних інфекцій.
19.10. КОНСУЛЬТУВАННЯ
Профілактичні заходи включають пропаганду захищеного сексу, боротьбу з наркоманією, дотримання санітарно-протиепідемічного режиму в медичних закладах, обстеження донорів тощо.
Для запобігання зараженню дітей потрібне планове обстеження вагітних на ВІЛ-інфекцію. При виявленні захворювання у вагітної слід призначити їй противірусне лікування, що знижує ризик захворюваності на дитину до 8%. Розродження ВІЧінфікованим жінкам проводять шляхом кесаревого розтину. Від грудного вигодовуваннядитину необхідно відмовитись.
Дерматовенерологія: підручник для студентів вищих навчальних закладів/В. В. Чеботарьов, О. Б. Тамразова, Н. В. Чеботарьова, А. В. Одинець. -2013. – 584 с. : іл.
Віч інфекція- повільно прогресуюче інфекційне захворювання, що виникає внаслідок зараження вірусом імунодефіциту людини.
ВІЛ вражає імунну систему, внаслідок чого організм стає високо сприйнятливим до опортуністичних інфекцій та пухлин, які в кінцевому підсумку призводять до загибелі хворого. Початкова назва ВІЛ-інфекції - СНІД (AIDS) – синдром набутого імунодефіциту.
Актуальність ВІЛ-інфекції.
Стрімке зростання наркоманії, статевого шляху інфікування, ураження ВІЛ молодих людей, інфікування дітей від матерів, низька ефективність лікувальних та відсутність специфічних засобів профілактики ставлять цю патологію на одне з перших місць в актуальності на сучасному періоді розвитку людства.
Історія. Вірус імунодефіциту людини (ВІЛ)був ідентифікований практично одночасно двома дослідниками: Люк Монтаньї (інститут Пастера – Франція) у 1983 (надалі визнаний ВІЛ-1) та у США в Національному інституті здоров'я Робертом Галло. Дата офіційної реєстрації СНІДу – 1981 рік, дослідження вірусологічного плану розпочалися саме з цього часу.
Характеристика збудника
Вірусологія. ВІЛ відноситься до сімейства ретровірусів, підродини лентивірусів Лентивіруси викликають хронічні інфекції з довгим латентним періодом, персистуючою репродукцією вірусу та ураженням ЦНС. ВІЛ-1 та ВІЛ-2 мають подібну структуру. У всьому світі більшість випадків СНІДу сьогодні спричинено ВІЛ-1. Число інфікованих ВІЛ-1 на земній кулі перевищує 40 млн. осіб, більшість із них живе в Азії, Західній, Екваторіальній та Південній Африці та Південній Америці.
Морфологія. Діаметр ВІЛ-1 становить 100 нм.. Зовні вірус оточений ліпідною мембраною, в яку вбудовано 72 глікопротеїдні комплекси. Кожен з цих комплексів утворений трьома молекулами поверхневого глікопротеїду (gpl20) та трьома трансмембранними (gp41). Всередині до ліпопротеїдної оболонки належить матриксний білок р 17. Серцевину вірусу (капсид) становить капсидний білок р24, який оточує білковонуклеїновий комплекс: дві молекули вірусної РНК, пов'язані з протеїдом р7 та зворотною транскриптазою рбб. Вірус містить усі необхідні ферменти для реплікації: зворотну транскриптазу, інтегразу р32 та протеазу pi 1. ВІЛ не стійкий у зовнішньому середовищі. Він інактивується при температурі 56 ° С за 30 хвилин, при кип'ятінні - через одну хвилину, гине під впливом хімічних агентів, допущених для проведення дезінфекції. Вірус щодо стійкий до іонізуючої радіації, ультрафіолетового опромінення та заморожування при - 70°С.
Шляхи передачі ВІЛ:
- при статевому контакті з ВІЛ-інфікованим;
- при переливанні інфікованої крові або продуктів крові (зараження можливе також при штучному заплідненні, трансплантації шкіри та органів);
- при використанні нестерильних голок та шприців, якими робив ін'єкції ВІЛ-інфікований;
- від матері дитині (під час вагітності, пологів та під час годуваннягрудьми, докладніше читайте сайт для мам http://formoms.com.ua/).
ВІЛ не передається:москітами, комарами, бліхами, бджолами та осами. ВІЛ не передається за побутових контактів. Не описано жодного випадку зараження через слину і слізну рідину, що не містять кров. Оскільки ВІЛ не передається зі слиною, не можна заразитися через загальні склянки, виделки, бутерброди чи фрукти (Friedland, 1986; Castro, 1988; Friedland, 1990). На думку провідних фахівців, потрапляння на непошкоджену шкіру інфікованих біологічних рідин (наприклад, крові) для передачі вірусу недостатньо.
Статеві контакти.
Статеві контакти без презервативу - найчастіший шлях передачі ВІЛ-інфекціїв усьому світі. Найвищий ризик зараження існує при пасивному анальному статевому контакті, проте описані випадки зараження після одноразового активного статевого контакту. Захворювання, що передаються статевим шляхом, значно підвищують ризик зараження ВІЛ. Чим нижче вірусне навантаження, тим менш заразний хворий.
Вживання ін'єкційних наркотиків.
Використання нестерилізованих шприців та голок, якими робив ін'єкції ВІЛ-інфікований, - важливий шлях передачі ВІЛ у країнах із великою кількістю споживачів ін'єкційних наркотиків. На відміну від випадкових уколів (при медичних маніпуляціях) голкою ризик зараження через загальні голки є набагато вищим, оскільки споживач ін'єкційних наркотиків перевіряє правильність положення голки, набираючи в неї кров.
Передача від матері до дитини (вертикальний шлях).
За відсутності профілактичних заходів частота передачі ВІЛ від матері дитині під час вагітностіта пологів становить 15-30%. Приблизно у 75% цих випадків передача ВІЛ відбувається на пізніх термінахвагітності та під час пологів. Близько 10% випадків вертикальної передачі ВІЛ відбувається у перших двох триместрах вагітності, ще 10-15% – під час грудного вигодовування.
В даний час вертикальна передача ВІЛ стає рідкістю завдяки антиретровірусній профілактиці та плановим кесаревим перерізам.
Ін'єкції та трансфузії інфікованих препаратів крові.
У більшості західних країн випадки трансфузії ВІЛ-інфікованої крові та її препаратів стали рідкістю. При сучасних методах діагностики та скринінгу донорської кровіризик зараження ВІЛ при переливанні однієї дози становить 1:1 ТОВ ТОВ.
Основні прояви епідемічного процесу.
- Перший етап (1987-1995 рр.) – завезення ВІЛ іноземними громадянами та поширення інфекції серед населення за рахунок сексуальних контактів, повільні темпи розвитку епідемічного процесу;
- Другий етап (1996-1998 р.р.) – стрімке поширення інфекції серед осіб, які вживають наркотичні речовини; провідний шлях передачі - парентеральний;
- Третій етап (1999 р. по теперішній час) – є наслідком попередньої, формується за рахунок сексуальних партнерів наркоспоживачів 1 осіб, інфікованих статевим шляхом. Вихід інфекції з груп ризику, зростає ризик інфікування жінок та дітей, що веде шлях передачі статевої.
Патогенез ВІЛ-інфекції.
Після проникнення вірусу в організм людини ВІЛ визначається у крові вже через 1-5 дібпісля зараження і з цього моменту інфікована людина стає джерелом інфекції. Тканини, в яких зосереджені клітини - мішені для ВІЛ є анатомічними резервуарами ВІЛ: лімфоїдна тканина, асоційована зі слизовими оболонками шлунково-кишкового тракту, респіраторного тракту та ін, лімфатичні вузли, тимус та кістковий мозок; Центральна нервова система; урогенітальний тракт, кров. Слизові оболонки ШКТ та інших органів містять близько половини всіх СБ4+лімфоцитів організму людини, і є первинним місцем реплікації ВІЛ вже в період гострої інфекції; З перших днів захворювання на ВІЛ-інфекцію є генералізованою інфекцією, тому що реплікація (відтворення) вірусу в інфікованих клітинах відбувається постійно, незалежно від клінічних проявів захворювання (латентна інфекція). Збудник здатний прямо інфікувати досить багато різних типів диференційованих клітин: насамперед Т4-лімфоцити (СБ4-хелпери), а також тимоцити, В-лімфоцити, клітини Лангерганса, моноцити/макрофаги, мегакаріоцити, еозинофіли, нейрони, нейроглі, судин, М-клітини слизової оболонки кишки, плаценту, можливо, поперечно-смугасту мускулатуру.
Виділяють кілька етапів реплікації ВІЛу сприйнятливих клітинах інфікованої людини.
- Зв'язування віріона із поверхнею клітини. Головним рецептором для ВІЛє рецептор CD4, основними корецептрами є хемокінові рецептори CXCR4 та CCR5.
- Злиття мембран віріону та клітини.
- Проникнення вірусу всередину клітини призводить до вивільнення нуклеотиду та геномної РНК вірусу, зворотної траскрипції геномної РНК ВІЛ та утворення ДНК (участь ферменту зворотної транскриптази). Синтез провірусної ДНК на матриці вірусної РНК у цитоплазмі клітини під дією ферменту зворотної транскриптази – це ключовий момент у репродукції ВІЛ.
- Інтеграція ДНК ВІЛ у геном інфікованої клітини (участь ферменту ВІЛ – інтегрази) – утворення ДНК провірусу ВІЛ.
- Активація транскрипції з ДНК провірусу та подальша транскрипція білків вірусу. напрацювання всіх компонентів вірусу з формуванням нових віріонів та їх вивільненням із клітини, (участь ферменту ВІЛ – протеази).
- Розтеплення молекул попередників протеазою ВІЛ необхідна умоваДля утворення нових вірусних частинок, цей фермент є ще однією мішенню для антиретровірусної терапії.
- Складання вірусів
Реплікація ретровірусів схильна до помилок і характеризується високою частотою спонтанних мутацій. Відмінною рисою ВІЛ є вибуховий характер процесів активації транскрипції, синтезу білків-попередників, складання віріонів та їх брунькування: за 5 хв одна лімфоцитарна клітина може утворити до 5000 вірусних частинок.
ВІЛ-інфекція призводить до ураження неспецифічного (вродженого імунітету) та специфічного клітинного та гуморального імунітету. Відбувається зниження вмісту та порушення функції центральних клітин імунітету - Т-хелперів (С04+лімфоцитів), ефекторних клітин імунної відповіді (натуральних кілерів, цитотоксичних С08+лімфоціів, регуляторних клітин). Розвивається хронічна активація імунної системи, що поступово призводить до глибокого імунодефіциту, нездатності контролювати опортуністичні інфекції, проліферативні процеси.
Симптоми ВІЛ-інфекції
При природному перебігу ВІЛ-інфекції виділяють 3 основні стадії:
- гостра фаза,
- латентна інфекція,
- стадія маніфестних проявів (пре-СНІД та СНІД).
Гостра інфекція(первинна інфекція або гострий ретровірусний синдром) – це результат початкової супресії Т-клітин. Стадія розвивається у більшості ВІЛ-інфікованих людей має клінічну картину інфекційного мононуклеозу або ознаки, які мають схожість із грипом. Найчастіше симптоми ВІЛ інфекції у чоловіків та жінок з'являються через 1-3 тижні після інфікування (цей період може подовжуватися до 10 місяців) і зберігаються в межах 1-6 тижнів (в середньому 14-21 день). Проявами гострого ретровірусного синдрому є лихоманка, біль у горлі, головний біль, міалгії та артралгії, нудота, блювання, діарея, лімфаденопатія. Часті клінічні симптоми ВІЛ у цій стадії хвороби є еритематозний або макулопапульозний висип на обличчі та тулубі, іноді на кінцівках. Неврологічна симптоматика може бути представлена у цю стадію менінгоенцефалітами, периферичною нейропатією, паралічем лицевого нерва, радикулопатією, психозами. Гематологічні порушення включають помірну лейкопенію, лімфопенію, тромбоцитопенію або відносний лімфоцитоз із появою атипових мононуклеарів. У цей період можна знайти транзиторне зниження CD4+ лімфоцитів. Рівень CD4+ клітин надалі підвищується, але з нормалізується Рівень віремії у період дуже високий. Виявлення антитіл до ВІЛ у цю стадію який завжди і найчастіше немає. Більш надійно визначати р24 антиген ВІЛ.
Латентна інфекція(асимптомна інфекція) слід за гострою фазою хвороби, і за відсутності симптомів захворювання на крові можливе виявлення ізолятів ВІЛ. Асимптомна інфекція (АІ) може тривати від 2 до 10 років. У цей період, незважаючи на інфікованість, людина залишається клінічно здоровою, у неї відсутні ознаки імунодефіциту. У цей період віремія ВІЛ мінімальна, CD4+ залишаються на рівні здорової людини. Тривалість АІ залежить від багатьох причин, насамперед від вихідного стану імунної системи людини, від наявності факторів, що негативно впливають на стан здоров'я інфікованого (наркоманія, алкоголізм, низький соціо- економічний статуста ін.). Персистуюча генералізована лімфаденопатія (ПГЛ). В даний час до асимптомної стадії відносять персистующую10 генералізовану лімфаденопатію (ПГЛ), т.к. вона найчастіше виявляється лише при лікарському обстеженні. Стадія ПГЛ розвивається при рівні CD4+ понад 500 кл/мкл і є результатом активації лімфоцитів. Головною клінічною ознакою є збільшення лімфатичних вузлів двох і більше груп (за винятком пахових), протягом трьох і більше місяців за відсутності іншої захворювання, яке могло б зумовлювати лімфаденопатію.
Стадії маніфестних проявів ВІЛ-інфекції (пре-СНІД, СНІД)виникають на тлі зростання віремії ВІЛ, зниження СД4+ і виявляються маніфестацією опортуністичних інфекцій та ВІЛ-асоційованих пухлин. Клінічні прояви ВІЛ-інфекції залежать від ступеня зниження імунітету, наявності різних варіантівкоінфекцій, генетичних особливостей індивіда. На ранніх симптомних стадіях (пре-СНІД) ВІЛ-інфекція проявляється ураженням слизових і шкіри (себорейний дерматит, орофарингеальний кандидоз, оніхомікози, локалізовані герпетичні ураження, лейкоплакія язика), рецидивуючими простудними, шкірними, урогенними >38,5°С, чи діарея тривалістю більше 1місяця, зниження маси тіла менш ніж на 10%). У пацієнтів діагностується клінічна категорія (класифікація CDC) або 2, 3 клінічна категорія (клінічна класифікація ВООЗ, 2006).
СНІД – термінальна стадія ВІЛ-інфекції, характеризується вираженим імунодефіцитом та/або маніфестацією важких опортуністичних інфекцій та пухлин. У пацієнта визначаються тяжкі атипово протікаючі інфекції (токсоплазмоз головного мозку, кандидозний езофагіт, кандидоз трахеї та бронхів, криптококоз, криптоспоридіоз, туберкульоз, атиповий мікобактеріоз, ВІЛ-деменція, ВІЛ-асоцімовані опухол. Розвивається виражене виснаження. У пацієнтів діагностується клінічна категорія С (класифікація CDC) або 4 клінічна категорія (клінічна класифікація ВООЗ, 2006).
Необхідно пам'ятати, що у багатьох пацієнтів стадія СНІДу тривалий час може протікати без типових клінічних проявів, за відсутності маніфестації ОІ та пухлин. Діагностика стадії СНІД у таких випадках можлива лише за імунологічними критеріями – визначення рівня СБ4+лімфоцитів (класифікація CDC). У таких випадках при зниженні показника нижче 200 кл/мкл діагностується стадія СНІДу, незалежно від клінічних проявів захворювання. Усі пацієнти на стадії СНІД повинні отримувати антиретровірусну терапію (APT) та профілактику ГІ та ОЗ.
Класифікація ВІЛ-інфекції.
В даний час у міжнародній клінічній практиці повсюдно використовується класифікація розроблена центром контролю за захворюваннями (CDC, Атланта, США, 1993) яка враховує клінічні та імунологічні (рівень ЦД4+) критерії.
Класифікація ВІЛ-інфекції (CDC, Атланта, США, 1993),
Клінічні групи
> 500 клітин на 1 мклА1В1С1
200-500 клітин на 1 мклА2В2С2
< 200 клеток в 1 мклАЗВЗСЗ
ВІЛ-інфекції визначається один із перерахованих станів: асимптомна ВІЛ-інфекція, що персистує генералізована лімфоаденопатія (ПГЛ) гостра (первинна) ВІЛ-інфекція.
До категорії В відносяться пацієнти, у яких не виявляються стану характерні для категорії С, і у яких спостерігається хоча б один із перерахованих станів: дисплазія або карцинома аноректального сквамозного епітелію, бацилярний ангіоматоз, орофарингеальний кандидоз кандидозний вульвовагініт (персистуючий, часто рецидивуючий або погано піддається лікуванню), конституційні симптоми (лихоманка >38,5°С, або діарея щонайменше два окремі епізоди, або протікає з ураженням більше одного дерматому), ідіопатична тромбоцитопенічна пурпура, листериоз, ВІЛ-асоційована нефропатія, оніхомікоз, запальні захворювання малого таза (особливо ускладнені тубооваріальним абсцесом), периферична нейропат.
Хоча більшість із включених до цього переліку захворювань не загрожують життю пацієнта, всі вони пов'язані з дефектом клітинного імунітету.
До категорії С відносяться пацієнти, у яких виявляються наступні захворювання і стани: кандидоз бронхів, трахеї або легень, кандидозний езофагіт, інвазивний рак шийки матки, кокцидіоідомікоз дисемінований або екстрапульмональний, криптококкоз екстрапульмональний, криптоспоридіоз хрон (з ураженням не тільки печінки, селезінки або лімфатичних вузлів), цитомегаловірусний ретиніт (з втратою зору), ВІЛ-деменція, герпетична інфекція (хронічні виразки, що не гояться більше 1 місяця, або бронхіт, пневмоніт, езофагіт, гістоплазмоз дис хронічний кишковий (тривалістю більше 1 місяця), саркома Капоші, лімфома Беркітта, імунобласна лімфома, первинна лімфома мозку, атипові мікобакгеріози дисеміновані або позалегеневі, туберкульоз будь-якої локалізації (легеневої або позалегеневої), пневмоцієнт льтифокальна лейкоенцефалопатія, рецидивна сальмонельозна септицемія, токсоплазмоз мозку, ВІЛ-кахексія.
Всі пацієнти в групах АЗ, ВЗ, С1-3 розцінюються як пацієнти, які потенційно потребують антиретровірусної терапії.
У зв'язку з проблемами у визначенні показника СЕ4+лімфоцитів у ряді регіонів світу ВООЗ розробила клінічну класифікацію ВІЛ у дорослих та підлітків (перегляд 2006 р.) без урахування даного показника. У даній класифікації виділено гостру ВІЛ-інфекцію та клінічні категорії хронічної ВІЛ-інфекції:
Клінічна класифікація ВІЛ-інфекціїу дорослих та підлітків (перегляд 2006 р.)
Гостра ВІЛ-інфекція
- асимптомна
- гострий ретровірусний синдром
- безсимптомна ВІЛ-інфекція
- персистуюча генералізована лімфаденопатія
Себорейний дерматит, анулярний хейліт, рецидивні виразкові ураження слизової порожнини рота, HZ (широкий процес уздовж одного дерматома), рецидивні інфекції респіраторного тракту (2 і більше епізодів за 6 місяців синуситів, середнього отиту, бронхіту, фарингіту, трахеїту), оніхомікози, папуза.
Волосиста лейкоплакія язика,невмотивована хронічна діарея, тривалістю більше 1 місяця, рецидивуючий оральний кандидоз (2 і більше епізоду за будь-які 6 місяців), тяжкі імовірно бактеріальні інфекції (пневмонія, емпієма), гострий некротичний виразковий стоматит, гінгівіт або періодонтит.
Легеневий туберкульоз, позалегеневий туберкульоз, невмотивована втрата ваги (більше 10% за 6 місяців), ВІЛ вастинг-синдром, пневмоцистна пневмонія, рецидивна важка рентгенологічно підтверджена пневмонія (2 і більше епізоду за рік), ЦМВ-ретин простого герпесу (хронічна або персистуюча протягом 1 міс. і більше), ВІЛ-асоційована кардіопати, інфекція нетуберкульозні мікобактеріальні інфекції або дисемінований атиповий мікобактеріоз.
Клінічна категорія А (за класифікацією CDC) відповідає гострій ВІЛ-інфекції та 1 клінічній категорії (за клінічною класифікацією ВООЗ), клінічна категорія В – 2 та 3 клінічним категоріям, клінічна категорія С – 4 категорії, відповідно.
У клінічній практиці в РБ використовується одночасно 2 класифікації: клінічна класифікація, 2006 та класифікація СДС, 1993. Крім того, вказується стадія перебігу ВІЛ-інфекції(АІ, пре-СНІД, СНІД).
Діагностика ВІЛ-інфекції.
Своєчасна діагностика ВІЛ-інфекціїдозволяє запобігти ускладненням, пов'язаним із пізньою стадією ВІЛ-інфекції, знизити ризик трансмісії ВІЛ-інфекції, своєчасно призначити ВААРТ, знизити захворюваність та летальність ВІЛ-інфікованих хворих.
Проте рання діагностика ВІЛ-інфекціїє проблемою у всьому світі. Так, за даними центру з контролю захворюваності, Атланта, у 41%. ВІЛ-інфікованиххворих на СНІД розвивається протягом 1 року після встановлення діагнозу, що ускладнює запобігання несприятливим результатам.
Усі діагностичні тести на ВІЛможна умовно поділити на 2 групи:
1. Тести, що дозволяють встановити факт інфікування ВІЛ
- Тести, що дозволяють контролювати перебіг (моніторинг) ВІЛ-інфекції у інфікованої людини (встановити стадію ВІЛ-інфекції, визначити показання на початок терапії, оцінити ефективність терапії).
2. Встановлення факту інфікованості ВІЛ.
1. Серологічні випробування:
- визначення антитіл до ВІЛ (ІФА, імуноблот)
- визначення антигену Р24
2. Молекулярно-генетичні випробування:
- Визначення РНК вірусу
- Визначення ДНК провірусу
У звичайній (рутинній) практиці для діагностики ВІЛ використовується так званий стандартний протокол серологічного тестування ВІЛ, у якому використовуються доступні та високоточні тести. Протокол включає проведення діагностики ВІЛ у 2 етапи: 1-й етап (скринінговий) - визначення антитіл до ВІЛ методом ІФА та при отриманні позитивних результатіввиконують 2 етап (підтверджує тест) - імуноблот, який дозволяє визначити наявність АТ до кількох антигенів: серцевини - Р17, Р24, Р55, оболонки - GPL20, 160, 41, ферментів - РЗ 1, Р51, РББ). Чутливість протоколу – 98-99,8%, специфічність – 99,994%
Проблема діагностичного вікна. Одна з найважливіших проблем тестування на ВІЛ – так званий період діагностичного вікна. Це термін, який проходить з моменту зараження ВІЛ до появи певного рівня антитіл (Busch 1997). Сучасні скринінг-тести виявляють ВІЛ-інфекцію через 38 днів після зараження. Вкрай рідко ВІЛ-інфекція виявляється лише через 3-6 місяців після зараження. Щоб скоротити період діагностичного вікна, у скринінг-тестах четвертого покоління визначаються антитіла до ВІЛ, антиген р24.
Прямі тести на ВІЛ. Діагноз ВІЛ-інфекції можна поставити не лише на підставі непрямих ознак (наявності антитіл до ВІЛ), а й на підставі прямих доказів присутності вірусу. До прямих тестів відносять:
- Виділення вірусу в культурі клітин - дослідження, яке зберігають для особливих випадків: воно вимагає спеціального обладнання та підготовки; у клінічній практиці не використовується.
- Тест на антиген р24 (скринінг-тести четвертого покоління, крім антитіл до ВІЛ, виявляють і антиген р24);
- Вірусні нуклеїнові кислоти (тобто генетичний матеріал ВІЛ) провірусну кДНК у лейкоцитах, вірусну РНК.
У зв'язку з можливістю отримання хибнопозитивних та хибнонегативних результатів при серологічному тестуванні на ВІЛ у частині обстежуваних застосовуються молекулярно-генетичні методи тестування – визначення вірусної РНК або провірусної ДНК ВІЛ методом ПЛР.
Пацієнти, яким проводиться діагностика ВІЛ із застосуванням ПЛР:
- новонароджені
- хворі з агаммаглобулінемією
- хворі, що перебувають у періоді «серологічного вікна»
- гостра ретровірусна інфекція
- донори крові.
У РБ будь-який бажаючий може пройти анонімне обстеження на ВІЛ-інфекцію у будь-якій медичній установі. Пацієнту гарантується повна конфендиційність, що охороняється законом РБ. Крім того, хворі обстежуються за клінічними показаннями за наявності ознак захворювань підозрілих на прояв ВІЛ. Контингенти, які підлягають обов'язковому тестуванню на ВІЛ визначено у наказі М3 РБ №351, 1998.
Контингенти, що підлягають обстеженню на ВІЛ у РБ (Службовий лист М3 РБ 18.12.2009 № 02-2-04/4037 «Про медичний огляд на ВІЛ»)
- Донори, іноземні громадяни, особи з клінічнимисимптомами захворювань (лихоманка, лімфаденопатія, втрата маси тіла, рецидиви пневмоній, серозний менінгіт невстановленої етіології, енцефаліт невстановленої етіології, нейропатії, недоумство та ін.). Хворі з підозрою або підтвердженим діагнозом (рецидиви бактеріальних інфекцій, кандидоз, криптококоз, туберкульоз, сепсис, саркома, мононуклеоз, утворення головного мозку, лімфоми та ін.). Новонароджені із затримкою розвитку, аномалії, маловагові, маса менше 2500. Хворі на парентеральні гепатити, вагітні, реципієнти препаратів крові, рідин, діти, народжені ВІЛ-інфікованими, діти на держзабезпеченні, особи з ІПСШ, наркомани, пенітенціарна система,
Дослідження, що дають змогу здійснювати моніторинг ВІЛ-інфекції.
- Визначення рівня лімфоцитів CD4+B у сироватці крові (імунограма методом моноклональних антитіл)
- Визначення вірусного навантаження ВІЛ у крові інфікованого (ПЛР)
- Визначення мутацій резистентності ВІЛ до антиретровірусних препаратів (ПЛР, генетичний аналіз ВІЛ).
- Визначення рівня лімфоцитів CD4+ у сироватці крові (імунограма методом моноклональних антитіл).
Цей метод дозволяє визначити стан імунної системи інфікованої людини. Рівень С04+лімфацитів є одним з найважливіших лабораторних показників для вирішення питання про призначення ВААРТ та для оцінки ефективності терапії, що проводиться. Нормальні діапазони рівня С04+лімфоцитів у дорослих перебувають у межах 500-1400 один мкл.
У разі відсутності можливості визначення показника С04+лімфоцитів (дослідження є дорогими та вимагають спеціально обладнаної лабораторії) при вирішенні питання призначення APT допустимо орієнтуватися на абсолютну кількість лімфоцитів у загальному аналізі крові. Показанням до призначення Ваарт є абсолютна кількість лімфоцитів менше 1,0 х 10 /л.
Визначення вірусного навантаження (ВГ) ВІЛ у крові інфікованого (ПЛР). Дослідження так званого вірусного навантаження сьогодні в клінічній практиці незамінне: воно дозволяє як оцінювати прогноз, так і слідкувати за ефективністю лікування. Знання вихідного (до початку ВААРТ) рівня ВН пацієнта є додатковим критерієм початку ВААРТ. Вважається, що рівень ВН вище 100 000 копій/мл – пороговий рівень для старту терапії у дорослих та дітей старше 1 року життя. Моніторинг ВН на тлі Ваарт є критерієм ефективності терапії. Так, при ефективній терапії рівень ВН повинен знижуватися та досягати невизначеного рівня (менше 50 копій/мл).
Експрес-тести на ВІЛ. Сьогодні випускається багато експрес-тестів на ВІЛ. Вони відомі як «тест на місці», «тест біля ліжка хворого» та "спрощений експрес-тест". В їх основі лежить один із чотирьох методів-реакція аглютинації, ІФА на полімерних мембранах (тест-смужки) імунологічний фільтраційний аналіз або імунохроматографія (Giles 1999, Branson 2000). Більшість таких тестів дає змогу отримати результат через 15-30 хвилин. Подібні експрес-тести корисні, коли результат необхідно отримати швидко, наприклад, у приймальному відділенні перед терміновими хірургічними втручаннями, пологами або після випадкової травми голкою. Основною проблемою застосування експрес-тестів – необхідність консультувати пацієнта перед тестуванням та отримувати його згоду на проведення тесту.
Лікування ВІЛ-інфекції. ВААРТ: поняття, цілі, принципи проведення
В даний час для лікування ВІЛ-інфікованих хворих використовується Високо Активна Антиретровірусна Терапія (ВААРТ) або Антиретровірусна Терапія (APT), яка представляє комбінацію 3 та більше антиретровірусних препаратів з різних груп. ВААРТ була впроваджена у широку клінічну практику з 1996 р., що дозволяє виділяти еру ВААРТ у лікуванні ВІЛ-інфікованих хворих та еру до ВААРТ (період до 1996 р.), коли широко застосовувалася монотерапія. В даний час монотерапія зидовудином використовується тільки у новонароджених з невідомим ВІЛ-статусом у перші 4 тижні життя для профілактики перинатального зараження ВІЛ.
Повсюдне використання ВААРТ призвело до значного зниження летальності ВІЛ-інфікованих хворих, зменшення частоти розвитку СНІДу та асоційованих з ним станів (опортуністичні інфекції, пухлини тощо). Результатом ВААРТ стало суттєве подовження тривалості життя та підвищення його якості.
Завдання антиретровірусної терапії - придушити репродукцію ВІЛ, знизити концентрацію вірусної РНК до невизначеної та підтримувати на такому рівні якнайдовше, зберегти або відновити функцію імунної системи, звести до мінімуму побічні ефекти APT.
Мета ВААРТ можна досягти лише при довічному застосуванні АРП і дуже ретельному дотриманні режиму терапії. Недотримання режиму ВВАРТ призводить до швидкого формування перехресної стійкості до вірусу АРП.
ВААРТ дозволяє радикально вилікувати хворого, тобто. домогтися повної ерадикації збудника з інфікованого організму пацієнта. Хворі, що перебувають на ВААРТ, залишаються джерелом ВІЛ-інфекції для сприйнятливих людей, хоча ефективна терапія знижує ступінь «заразності» ВІЛ-інфікованого пацієнта, оскільки призводить до зниження рівня віремії ВІЛ у крові та тканинах хворого, аж до невизначеного.
Показання для призначення ВААРТ. Відповідно до рекомендацій ВООЗ, ВААРТ призначається пацієнтам з підтвердженим діагнозом ВІЛ-інфекції залежно від клінічної та імунологічної стадії ВІЛ.
Починати ВААРТ рекомендується за наявності маніфестної стадії ВІЛ-інфекції (клінічні стадії В та С за класифікацією CDC), зниження рівня лімфоцитів СЕ4-ь<350/мкл и повышения уровня вирусной нагрузки ВИЧ в крови инфицированного более 100000 коп/мкл.
В даний час для лікування ВІЛ використовується високоактивнаантиретровірусна терапія (ВААРТ), яка є комбінацією 3 і більше антиретровірусних препаратів (АРП) з різних груп.
1 група АРП – нуклеозидні інгібітори зворотної транскриптази (НДПТ). НДПТ конкурують з природними нуклеозидами, аналогами яких вони є і від яких відрізняються лише невеликою зміною в структурі молекули, що порушує здатність утворювати фосфодіефірний зв'язок, який необхідний для побудови та стабілізації подвійного ланцюга ДНК, що призводить до зупинки синтезу провірусної ДНК. До НДВП відносять: Ретровір, Дивір, Ставір, Епівір, Зіаген, Тенофавір, Емтрицитабін.
2 група АРП – ненуклеозидні інгібітори зворотної транскриптази (ННІОТ). На відміну від НДПТ, засоби цієї групи не виступають як «підроблений» будівельний матеріал, а безпосередньо неконкурентно пов'язуються зі зворотною транскриптазою. До ННІОТ відносять: Делавердін, Невірапін, Ефавір.
3 група АРП – інгібітори протеази (ІП). ІП вбудовуються в активну ділянку протеази ВІЛ, що призводить до порушення вірусної мРНК, внаслідок чого утворюються вірусні частки, не здатні заражати нові клітини. До ІП відносять: Індинавір Інвіраза, Нелфінавір, Норвір, Калерта, Фортаваза, Азатановір, Фосампренавір, Даруновір, Тіпрановір.
4 група АРП – інгібітори фузії (ІФ). Препарат зв'язується з проміжною структурою білка зовнішньої оболонки ВІЛ-gp41, який з'являється на поверхні вірусу, коли він зливається з мембраною клітини-мішені, тим самим інгібує механізм злиття ВІЛ з клітиною. До ІФ відносять: Енфувіртид.
5 група АРП – інгібітор інтегрази (ІІ). Препарат блокує фермент вірусу, що бере участь у вбудовуванні провірусної ДНК у геном клітини-мішені. До ІІ відносять: Ралтегравір.
Ефективність ВААРТ безпосередньо залежить від дотримання режиму прийому препаратів: дозування, кратність прийому, залежність від їжі для деяких препаратів. Комплаєнс - це дотримання хворим на режим прийому ВААРТ.
Лікування опортуністичних інфекцій. Призначається специфічна етіотропна терапія залежно від нозологічної форми захворювання (протитуберкульозна, протигерпетична, антибактеріальна, хіміо- та променева терапія тощо). Необхідно пам'ятати, що при ряді опортуністичних захворювань відсутня можливість етіотропної терапії (мультифокальна лейкоенцефалопатія, аногенітальні кондиломи, волосяна лейкоплакія язика тощо). У разі основним видом терапії є своєчасне призначення ВААРТ.
Профілактика ОІ є обов'язковим і одним із найважливіших компонентів спостереження та ведення хворих із ВІЛ-інфекцією. Існує ряд ОІ, для профілактики яких має призначатися обов'язкова медикаментозна профілактична терапія залежно від рівня ІС та показника CD4+.
Виділяють первинну профілактику ОІ та вторинну.
- Первинна профілактика – спрямована на попередження виникнення ОІ у ВІЛ-інфікованого хворого.
- Вторинна профілактика – спрямована на попередженнявиникнення рецидиву ОІ після перенесеної ОІ у ВІЛ-інфікованогопацієнта.
Показання до обов'язкової первинної профілактики інфікованих залежать від клінічних та імунологічних критеріїв:
- пневмоцистна пневмонія – при зниженні CD4+<200 кл/млили
- наявності кандидозу порожнини рота та глотки (триметопримом/сульфометоксазолом,пентамідин, кліндаміцин, атаваквон);
- туберкульоз - при позитивній туберкуліновій пробі (>5мм) абоконтакт з хворим на активний туберкульоз (ізоніазид, рифампіцин);
- токсоплазмоз – при зниженні CD4+кл/мл
- (триметопримом/сульфометоксазол, дапсон);
- атиповий мікобактеріоз – при зниженні CD4+<50 кл/мл (азитромицин, кларитромицин);
- криптококоз - при зниженні CD4+<50 кл/мл (флюконазол). Профилактика и мероприятия в очаге. Важное значение в поширення ВІЛ-інфекції має пропаганда здорового способу життя (обмеження кількості статевих партнерів та використання презервативів).
З метою профілактики парентерального шляху зараження проводиться регулярне виявлення джерел ВІЛ, обстеження донорів крові, органів, сперми, а також осіб із групи ризику. У медичних закладах повинні ретельно стерилізувати інструментарій, використовувати одноразові шприци та голки.
Під час перебування ВІЛ-інфікованого у сім'їнеобхідно підтримувати належний санітарно-гігієнічний режим.
Медичним працівникам слід ретельно дотримуватись заходів попередження зараження ВІЛ при проведенні парентеральних лікувальних та діагностичних маніпуляцій. Медичні працівники з травмами (пораненнями на руках, ексудативними ураженнями шкіри) усуваються від медичного обслуговування хворих, контакту з предметами догляду за ними. Щоб уникнути поранень при заборі крові та інших біологічних рідин, неприпустимо використання скляних предметів з відбитими краями. Зразки крові (сироватки) повинні доставлятися до лабораторії у герметично закритих гумовими пробками пробірках, поміщених у штативи та упакованих у контейнери. Не допускається розміщення бланків або іншої документації у контейнер. Будь-яке пошкодження шкіри, слизових оболонок, забруднення їх біологічними матеріалами пацієнтів під час надання їм медичної допомоги має розцінюватися як контакт із матеріалом, що містить ВІЛ.
Розбирати, мити та прополіскувати медичні інструментарії, піпетки, лабораторний посуд, що стикалися з кров'ю або сироваткою людей слід після попередньої дезінфекції та у гумових рукавичках.
При контакті з кров'ю або іншими біологічними матеріалами з порушенням цілісності шкіри (укол, поріз), потерпілий повинен зняти рукавички робочою поверхнею всередину, видавити кров з рани, обробити пошкоджене місце 70% спиртом або 5% настоянкою йоду при порізах, розчином пероксиду водню при уколах. Потім треба вимити руки з милом під проточною водою і протерти 70% спиртом, на рану накласти пластир, надягти напальчник і при необхідності продовжити роботу, одягнувши нові рукавички.
У разі забруднення кров'ю або сироваткою робочого столу слід негайно двічі обробити його засобами, що дезінфікують: відразу після забруднення, а потім через 15 хвилин. Якщо внаслідок пошкодження шкіри або слизових оболонок медичного працівника стався контакт із кров'ю або рідинами інфікованого організму, необхідно вдатися до посттравматичної профілактики за допомогою антиретровірусних засобів. Комбінована хіміопрофілактика обов'язкова протягом чотирьох тижнів: прийом трьох препаратів - двох інгібіторів ОТ (азідотімідин і ламівудін) та одного інгібітора протеази (лопіновір).
17/08/2012 15:30 Хламідійні інфекції – Визначення, актуальність, характеристика збудника, епідеміологія, клініка, ускладнення, діагностика, лікування, профілактика. -
Являє собою захворювання, яке викликається вірусом імунодефіциту людини, що характеризується синдромом набутого імунодефіциту, що сприяє виникненню вторинних інфекцій та злоякісних утворень у зв'язку з глибоким пригніченням захисних властивостей організму. ВІЛ-інфекція має різноманітні варіанти перебігу. Захворювання може тривати лише кілька місяців або розтягуватися до 20 років. Основним способом діагностики ВІЛ-інфекції залишається виявлення специфічних противірусних антитіл, а також вірусної РНК. В даний час лікування пацієнтів з ВІЛ проводиться антиретровірусними препаратами, здатними знижувати репродукцію вірусу.
Загальні відомості
Являє собою захворювання, яке викликається вірусом імунодефіциту людини, що характеризується синдромом набутого імунодефіциту, що сприяє виникненню вторинних інфекцій та злоякісних утворень у зв'язку з глибоким пригніченням захисних властивостей організму. Сьогодні у світі відзначається пандемія ВІЛ-інфекції, захворюваність населення планети, особливо країн Східної Європи, неухильно зростає.
Характеристика збудника
Вірус імунодефіциту людини ДНК містить, що відноситься до роду Lentivirus сімейства Retroviridae. Розрізняють два типи: ВІЛ-1 є основним збудником ВІЛ-інфекції, причиною пандемії, розвитку СНІДу. ВІЛ-2 – малопоширений тип, що зустрічається в основному в Західній Африці. ВІЛ – нестійкий вірус, швидко гине поза організмом носія, чутливий до впливу температури (знижує інфекційні властивості при температурі 56 °С, гине через 10 хвилин при нагріванні до 70-80 °С). Добре зберігається у крові та її препаратах, підготовлених для переливання. Антигенна структура вірусу дуже мінлива.
Резервуаром і джерелом ВІЛ-інфекції є людина: страждає на СНІД і носій. Природних резервуарів ВІЛ-1 не виявлено, є думка, що природним господарем у природі є дикі шимпанзе. ВІЛ-2 переноситься африканськими мавпами. Сприйнятливість до ВІЛ в інших видів тварин не відзначено. Вірус міститься у високих концентраціях у крові, спермі, секреті вагінальних залоз та менструальних виділеннях. Може виділятися з жіночого молока, слини, слізного секрету та ліквору, але ці біологічні рідини становлять меншу епідеміологічну небезпеку.
Імовірність передачі ВІЛ-інфекції підвищується за наявності пошкоджень шкірних покровів та слизових оболонок (травми, садна, ерозія шийки матки, стоматит, парадонтоз та ін.) ВІЛ передається за допомогою гемоконтактного та біоконтактного механізму природним шляхом (при статевих контактах та вертикально) дитині) та штучній (переважно реалізується при гемоперкутанному механізмі передачі: при трансфузіях, парентеральних введеннях речовин, травматичних медичних процедурах).
Ризик ураження ВІЛ при одиничному контакті з носієм невисокий, регулярні статеві контакти з інфікованим його значно підвищують. Вертикальна передача інфекції від хворої матері дитині можлива як у внутрішньоутробному періоді (через дефекти плацентарного бар'єру), так і під час пологів, при контакті дитини з кров'ю матері. У поодиноких випадках фіксується постнатальна передача з грудним молоком. Захворюваність серед дітей у заражених матерів сягає 25-30%.
Парентеральне зараження відбувається при ін'єкціях за допомогою голок, забруднених кров'ю ВІЛ-інфікованих осіб, при гемотрансфузіях зараженої крові, нестерильних медичних маніпуляціях (пірсинг, татуювання, медичні та стоматологічні процедури, що виробляються інструментарієм без належної обробки). Контактно-побутовим шляхом ВІЛ не передається. Сприйнятливість людини до ВІЛ-інфекції – висока. Розвиток СНІД в осіб старше 35 років, як правило, відбувається в короткі терміни з моменту зараження. У деяких випадках відзначається несприйнятливість до ВІЛ, що пов'язують із специфічними імуноглобулінами А, присутніми на слизових оболонках статевих органів.
Патогенез ВІЛ-інфекції
Вірус імунодефіциту людини при попаданні в кров впроваджується в макрофаги, мікроглію та лімфоцити, що мають важливе значення у формуванні імунних реакцій організму. Вірус знищує здатність імунних тілець до розпізнавання своїх антигенів як чужорідних, заселяє клітину та приступає до репродукції. Після виходу вірусу, що розмножився, в кров, клітина-господар гине, а віруси впроваджуються в здорові макрофаги. Синдром розвивається повільно (роками), хвилеподібно.
Перший час організм компенсує масову загибель імунних клітин, виробляючи нові, з часом компенсація стає недостатньою, кількість лімфоцитів і макрофагів у крові значно знижується, імунна система руйнується, організм стає беззахисним як по відношенню до екзогенної інфекції, так і до бактерій, що населяють органи та тканини. у нормі (що веде до розвитку опортуністичних інфекцій). Крім того, порушується механізм захисту від розмноження дефектних бластоцитів – злоякісних клітин.
Заселення вірусом імунних клітин часто провокує різні аутоімунні стани, зокрема характерні неврологічні розлади в результаті аутоімунного ураження нейроцитів, які можуть розвинутись навіть раніше, ніж проявиться клініка імунодефіциту.
Класифікація
У клінічному перебігу ВІЛ-інфекції розрізняють 5 стадій: інкубації, первинних проявів, латентна, стадія вторинних захворювань та термінальна. Стадія первинних проявів може протікати безсимптомно, як первинної ВІЛ-інфекції, а також поєднуватися з вторинними захворюваннями. Четверта стадія залежно від тяжкості поділяється на періоди: 4А, 4Б, 4В. Періоди проходять фази прогресування та ремісії, що різняться залежно від наявної протиретровірусної терапії або її відсутності.
Симптоми ВІЛ-інфекції
Стадія інкубації (1)- може становити від 3 тижнів до 3 місяців, в окремих випадках подовжується до року. У цей час триває активне розмноження вірусу, але імунна відповідь на нього поки що відсутня. Інкубаційний період ВІЛ закінчується або клінікою гострої ВІЛ-інфекції, або появою у крові ВІЛ-антитіл. На цій стадії основою діагностики ВІЛ-інфекції є виявлення вірусу (антигенів або частинок ДНК) у сироватці крові.
Стадія первинних проявів (2)характеризується проявом реакції організму на активну реплікацію вірусу у вигляді клініки гострої інфекції та імунної реакції (вироблення специфічних антитіл). Друга стадія може протікати безсимптомно, єдиною ознакою ВІЛ-інфекції, що розвивається, буде позитивна серологічна діагностика на антитіла до вірусу.
Клінічні прояви другої стадії протікають на кшталт гострої ВІЛ-інфекції. Початок гострий, відзначається у 50-90% пацієнтів через три місяці після моменту зараження, часто передуючи формуванню ВІЛ-антитіл. Гостра інфекція без вторинних патологій має досить різноманітний перебіг: можуть відзначатися лихоманка, різноманітні поліморфні висипання на шкірних покривах та видимих слизових оболонках, полілімфаденіт, фарингіт, лієнальний синдром, діарея.
У 10-15% хворих гостра ВІЛ-інфекція протікає із приєднанням вторинних захворювань, що пов'язано зі зниженням імунітету. Це можуть бути ангіни, пневмонії різного генезу, грибкові інфекції, герпес та ін.
Гостра ВІЛ-інфекція зазвичай триває від кількох днів до кількох місяців, в середньому 2-3 тижні, після чого в переважній більшості випадків переходить у латентну стадію.
Латентна стадія (3)характеризується поступовим наростанням імунодефіциту. Загибель імунних клітин у цій стадії компенсується їх підвищеним виробництвом. У цей час діагностувати ВІЛ можна за допомогою серологічних реакцій (у крові присутні антитіла до ВІЛ). Клінічною ознакою може бути збільшення кількох лімфатичних вузлів із різних, не пов'язаних між собою груп, крім пахових лімфовузлів. При цьому інших патологічних змін з боку збільшених лімфовузлів (болючість, зміни оточуючих тканин) не відзначається. Латентна стадія може тривати від 2-3 років до 20 і більше. У середньому вона триває 6-7 років.
Стадія вторинних захворювань (4)характеризується виникненням супутніх (опортуністичних) інфекцій вірусного, бактеріального, грибкового, протозойного генезу, злоякісних утворень на фоні вираженого імунодефіциту. Залежно від виразності вторинних захворювань розрізняють 3 періоди перебігу.
- 4А – втрата маси тіла не перевищує 10%, відзначаються інфекційні (бактеріальні, вірусні та грибкові) ураження покривних тканин (шкіри та слизових оболонок). Працездатність знижена.
- 4Б - втрати у вазі більше 10% загальної маси тіла, тривала температурна реакція, можлива тривала діарея, що не має органічної причини, може приєднуватися туберкульоз легень, інфекційні захворювання рецидивують і прогресують, виявляється локалізована саркома Капоші, волосиста.
- 4В – відзначається загальна кахексія, вторинні інфекції набувають генералізованих форм, відзначається кандидоз стравоходу, дихальних шляхів, пневмоцистна пневмонія, туберкульоз позалегеневих форм, дисемінована саркома Капоші, неврологічні розлади.
Підстадії вторинних захворювань проходять фази прогресування та ремісії, що різняться залежно від наявної протиретровірусної терапії або її відсутності. У термінальній стадії ВІЛ-інфекції вторинні захворювання, що розвинулися у хворого, набувають незворотного характеру, заходи лікування втрачають свою ефективність, летальний кінець настає через кілька місяців.
Перебіг ВІЛ-інфекції досить різноманітний, який завжди мають місце всі стадії, ті чи інші клінічні ознаки можуть бути відсутніми. Залежно від індивідуального клінічного перебігу тривалість захворювання може становити як кілька місяців, і 15-20 років.
Особливості клініки ВІЛ-інфекції у дітей
ВІЛ у ранньому дитячому віці сприяє затримці фізичного та психомоторного розвитку. Рецидивування бактеріальних інфекцій у дітей відзначають частіше, ніж у дорослих, часті лімфоїдні пневмоніти, збільшення легеневих лімфовузлів, різні енцефалопатії, анемія. Частою причиною дитячої смертності при ВІЛ-інфекціях є геморагічний синдром, що є наслідком вираженої тромбоцитопенії.
Найчастішим клінічним проявом ВІЛ-інфекції у дітей є затримка темпів психомоторного та фізичного розвитку. ВІЛ-інфекція, отримана дітьми від матерів анте- та перинатально протікає помітно важче і швидше прогресує, на відміну від такої у дітей, заражених після року.
Діагностика
В даний час основним діагностичним методом при ВІЛ-інфекції є виявлення антитіл до вірусу, що виробляється з застосуванням методики ІФА. У разі позитивного результату досліджують сироватку за допомогою методики імунного блоттингу. Це дозволяє ідентифікувати антитіла до специфічних антигенів ВІЛ, що є достатнім критерієм остаточного діагностування. Невиявлення за допомогою блоттингу антитіл характерної молекулярної маси не виключає ВІЛ. В інкубаційний період імунна відповідь на використання вірусу ще не сформована, а в термінальній стадії в результаті вираженого імунодефіциту антитіла перестають вироблятися.
При підозрі на ВІЛ та відсутності позитивних результатів імунного блоттингу ефективним методом виявлення частинок РНК вірусу є ПЛР. Діагностована серологічними та вірусологічними методами ВІЛ-інфекція є показанням до динамічного спостереження за станом імунного статусу.
Лікування ВІЛ-інфекції
Терапія ВІЛ-інфікованих осіб має на увазі постійний контроль імунного статусу організму, профілактику та лікування вторинних інфекцій, що виникають, контроль над розвитком новоутворень. Найчастіше ВІЛ-інфікованим особам потрібна психологічна допомога та соціальна адаптація. В даний час у зв'язку зі значним поширенням та високою соціальною значимістю захворювання в державних та світових масштабах здійснюється підтримка та реабілітація хворих, розширюється доступ до соціальних програм, що надають хворим медичну допомогу, що полегшує перебіг та покращує якість життя пацієнтів.
На сьогоднішній день переважним етіотропним лікуванням є призначення препаратів, що знижують репродуктивну здатність вірусу. До антиретровірусних препаратів відносяться:
- НДПТ (нуклеозидні інгібітори транскриптази) різних груп: зидовудин, ставудин, залцитабін, диданозин, абакавір, комбіновані препарати;
- НтІОТ (нуклеотидні інгібітори зворотної транскриптази): невірапін, ефавіренз;
- інгібітори протеази: ритонавір, саквінавір, даранавір, нелфінавір та інші;
- інгібітори злиття.
При прийнятті рішення про початок противірусної терапії пацієнтам слід пам'ятати, що застосування препаратів здійснюється багато років практично довічно. Успіх терапії безпосередньо залежить від суворого дотримання рекомендацій: своєчасного регулярного прийому лікарських засобів у необхідних дозуваннях, дотримання запропонованої дієти та суворе дотримання режиму.
Виникаючі опортуністичні інфекції лікують відповідно до правил ефективної проти збудника терапії, що викликав їх (антибактеріальні, протигрибкові, противірусні засоби). Імуностимулююча терапія при ВІЛ-інфекції не застосовується, оскільки сприяє її прогресу, цитостатики, що призначаються при злоякісних утвореннях, пригнічують імунітет.
Лікування ВІЛ-інфікованих включає загальнозміцнюючі та підтримуючі організм засоби (вітаміни та біологічно активні речовини) та методики фізіотерапевтичної профілактики вторинних захворювань. Хворим, які страждають на наркоманію, рекомендується лікування у відповідних диспансерах. У зв'язку зі значним психологічним дискомфортом багато пацієнтів проходять тривалу психологічну адаптацію.
Прогноз
ВІЛ-інфекція повністю невиліковна, у багатьох випадках противірусна терапія дає незначний результат. На сьогоднішній день у середньому ВІЛ-інфіковані живуть 11-12 років, проте ретельна терапія та сучасні лікувальні препарати дозволять помітно подовжити термін життя пацієнтів. Основну роль стримуванні СНІД, що розвивається, грає психологічний стан хворого і його зусилля, спрямовані на дотримання прописаного режиму.
Профілактика
В даний час Всесвітня організація охорони здоров'я проводить загальні профілактичні заходи щодо зниження захворюваності на ВІЛ-інфекцію за чотирма основними напрямками:
- просвітництво у питаннях безпеки статевих відносин, поширення презервативів, лікування захворювань, що передаються статевим шляхом, пропагування культури статевих взаємин;
- контроль за виготовленням препаратів з донорської крові;
- ведення вагітності ВІЛ-інфікованих жінок, забезпечення їх медичної допомоги та надання їм засобів хіміопрофілактики (в останньому триместрі вагітності та під час пологів жінки отримують антиретровірусні препарати, які також на перші три місяці життя призначаються новонародженим дітям);
- організація психологічної та соціальної допомоги та підтримки ВІЛ-інфікованих громадян, консультування.
В даний час у світовій практиці особливу увагу приділяють таким епідеміологічно важливим щодо захворюваності на ВІЛ-інфекцію факторів, як наркоманія, безладне статеве життя. Як профілактичний захід у багатьох країнах проводиться безплатна роздача одноразових шприців, метадонова замісна терапія. Як міра, що сприяє зниженню статевої неграмотності, у навчальні програми вводяться навчальні статевої гігієни курси.
Доброго часу, дорогі читачі!
У сьогоднішній статті ми розглянемо з вами таке серйозне захворювання, як – ВІЛ-інфекція, та все, що з ним пов'язано – причини, як передається, перші ознаки, симптоми, стадії розвитку, види, аналізи, тести, діагностику, лікування, ліки, профілактику та іншу корисну інформацію. Отже…
Що означає ВІЛ?
ВІЛ-інфекція у дітей
ВІЛ-інфекція у дітей у багатьох випадках супроводжується затримкою у розвитку (фізичного та психомоторного), часті інфекційні хвороби, пневмонітами, енцефалопатією, гіперплазією пульмональних лімфатичних улов, геморагічним синдромом. Більше того, ВІЛ-інфекція у дітей, яку вони придбали від інфікованих матерів, характеризується більш швидким перебігом та прогресуванням.
 Основна причина ВІЛ-інфекції – інфікування вірусом імунодефіциту людини. Причиною СНІД є той самий вірус, т.к. СНІД – остання стадія розвитку ВІЛ-інфекції.
Основна причина ВІЛ-інфекції – інфікування вірусом імунодефіциту людини. Причиною СНІД є той самий вірус, т.к. СНІД – остання стадія розвитку ВІЛ-інфекції.
– вірус, що повільно розвивається, відноситься до сімейства ретровірусів (Retroviridae) і до роду лентивірусів (Lentivirus). Саме слово «lente» у перекладі з латинської означає – «повільний», що частково і характеризує цю інфекцію, яка розвивається від моменту потрапляння в організм і до останньої стадії досить повільно.
Розмір вірусу імунодефіциту людини становить близько 100-120 нанометрів, що майже в 60 разів менше діаметра кров'яної частинки – еритроциту.
Складність ВІЛ полягає у його частих генетичних змінах у процесі самовідтворення – майже кожен вірус відрізняється від свого попередника хоча б на 1 нуклеотид.
У природі, станом на 2017 рік, відомі 4 види вірусу – ВІЛ-1 (HIV-1), ВІЛ-2 (HIV-2), ВІЛ-3 (HIV-3) та ВІЛ-4 (HIV-4), кожен з яких відрізняється структурою геному та іншими властивостями.
В основі хвороби більшості ВІЛ-інфікованих відіграє роль саме ВІЛ-1 інфекція, тому коли цифра підтипу не вказується, за умовчанням мається на увазі саме 1.
Джерело ВІЛ – інфіковані вірусом люди.
Основними шляхами зараження є: ін'єкції (особливо ін'єкційні наркотики), переливання (крові, плазми, еритроцитарної маси) або трансплантація органів, незахищений статевий контакт з малознайомою людиною, неприродний секс (анальний, оральний), травмування при пологах, вигодовування молоком. мати (інфікована), травмування під час пологів, використання не продезінфікованих медичних або косметологічних предметів (скальпель, голки, ножиці, машинки для тату, стоматологічних та інших інструментів).
Для інфікування ВІЛ та його подальшого поширення по організму та розвитку необхідно, щоб інфікована кров, слиз, сперма та інші біоматеріали хворого потрапили в кровоносне русло або лімфатичну систему людини.
Цікавим фактом є те, що у деяких людей в організмі є вроджений захист від вірусу імунодефіциту людини, тому вони стійкі до ВІЛ. Такі захисні властивості мають такі елементи - білок CCR5, білок TRIM5a, білок CAML (calcium-modulated cyclophilin ligand), а також інтерферон-індукований трансмембранний білок CD317/BST-2 («tetherin»).
До речі, білок CD317 крім ретровірусів також активно протидіє ареновірусам, філовірусам і герпесвірусам. Кофактор CD317 є клітинний білок ВСА2.
Групи ризику зараження ВІЛ
- Наркомани, які переважно вживають ін'єкційні наркотики;
- Статеві партнери наркоманів;
- Особи, що ведуть безладне статеве життя, а також ті, хто займається неприродним сексом;
- Повії та їх клієнти;
- Донори та люди, які потребують переливання крові або трансплантації органів;
- Хворі люди венеричними захворюваннями;
- Лікарі.
Класифікація ВІЛ-інфекції відбувається так:
Класифікація за клінічними проявами (у РФ та деяких країнах СНД):
 1. Стадія інкубації.
1. Стадія інкубації.
2. Стадія первинних проявів, яка за варіантами перебігу може бути:
- без клінічних проявів (безсимптомна);
- гострий перебіг без вторинних захворювань;
- гострий перебіг із вторинними захворюваннями;
3. Субклінічна стадія.
4. Стадія вторинних захворювань, зумовлених ураженням організму вірусами, бактеріями, грибком та інші види інфекції, що розвиваються і натомість ослабленого імунітету. По течії поділяється на:
А) маса тіла знижується на менше 10%, а також часто повторювані, інфекційні захворювання шкіри та слизових – фарингіти, середній отит, оперізуючий лишай, ангулярний хейліт ();
Б) маса тіла знижується більш ніж на 10%, а також стійкі та часто повторювані, інфекційні захворювання шкіри, слизових та внутрішніх органів – синусити, фарингіти, оперізуючий лишай, або діарея (пронос) протягом місяця, локалізована саркома Капоші;
В) маса тіла значно знижується (кахексія), а також стійкі генералізовані інфекційні захворювання дихальної, травної, нервової та інших систем – кандидози (трахеї, бронхів, легенів, стравоходу), пневмоцистна пневмонія, позалегковий туберкульоз, герпес, енцефалопатія, (Дисемінована саркома Капоші).
Всі варіанти перебігу 4 стадії мають наступні фази:
- прогресування патології за відсутності високоактивної антиретровірусної терапії (ВААРТ);
- прогресування патології і натомість ВААРТ;
- ремісія на фоні або після проведення ВААРТ.
5. Термінальна стадія (СНІД).
Наведена вище класифікація багато в чому співпадає з класифікацією, затвердженою Всесвітньою Організацією Охорони Здоров'я (ВООЗ).
Класифікація з клінічних проявів (CDC — Центр контролю та профілактики захворювань США):
Класифікація CDC включає не тільки клінічні прояви захворювання, але й показник числа CD4 + -Т-лімфоцитів в 1 мкл крові. В основі лежить поділ ВІЛ-інфекції лише на 2 категорії: сама хвороба та СНІД. Якщо наведені нижче параметри відповідають критеріям А3, В3, С1, С2 і С3, пацієнта враховують, як хворого на СНІД.

Симптоми в залежності від категорії CDC:
А (гострий ретровірусний синдром) – характеризується безсимптомним перебігом або генералізованою лімфаденопатією (ГЛАП).
(синдроми СНІД-асоційованого комплексу) – може супроводжуватися кандидозом ротової порожнини, оперізуючим герпесом, дисплазією шийки матки, периферичною нейропатією, органічним ураженням, ідіопатичною тромбоцитопенією, лейкоплакією або листериозом.
С (СНІД) – може супроводжуватися кандидозом дихальних шляхів (від ротоглотки до легень) та/або стравоходу, пневмоцистозом, пневмоніями, герпетичним езофагітом, ВІЛ-енцефалопатією, ізоспорозом, гістоплазмозом, мікобактеріозом, цитомеозою Капоші, лімфомою, сальмонельозом та іншими захворюваннями.
Діагностика ВІЛ-інфекції
Діагностика ВІЛ-інфекції включає такі методи обстеження:
- Анамнез;
- візуальний огляд пацієнта;
- Скринінг-тест (виявлення антитіл крові до інфекції методом імуноферментного аналізу – ІФА);
- Підтверджує наявність антитіл у крові тест (дослідження крові методом імунного блоттингу (блоту)), який проводиться лише за позитивного результату скринінг-тесту;
- Полімеразна ланцюгова реакція (ПЛР);
- Аналізи на імунний статус (підрахунок CD4 + лімфоцитів – проводиться за допомогою автоматичних аналізаторів (метод проточної цитометрії) або вручну за допомогою мікроскопів);
- Аналіз на вірусне навантаження (підрахунок кількості копій РНК ВІЛ у мілілітрі плазми);
- Експрес-тести на ВІЛ – діагностика проводиться за допомогою ІФА на тест-смужках, реакції аглютинації, імунохроматографії чи імунологічного фільтраційного аналізу.
Для встановлення діагнозу СНІД одних тестів недостатньо. Підтвердження відбувається лише за додаткової наявності 2-х і більше асоційованих із цим синдромом опортуністичних захворювань.

ВІЛ-інфекція - лікування
 Лікування ВІЛ-інфекції можливе лише після ретельної діагностики. Проте, на жаль, станом на 2017 рік офіційно адекватної терапії та лікарських препаратів, які б повністю усунули вірус імунодефіциту людини та вилікували хворого не встановлені.
Лікування ВІЛ-інфекції можливе лише після ретельної діагностики. Проте, на жаль, станом на 2017 рік офіційно адекватної терапії та лікарських препаратів, які б повністю усунули вірус імунодефіциту людини та вилікували хворого не встановлені.
Єдиним сучасним методом лікування ВІЛ-інфекції на сьогоднішній день є високоактивна антиретровірусна терапія (ВААРТ), яка спрямована на уповільнення прогресування захворювання та зупинення його переходу зі стадію СНІД. Завдяки ВААРТ життя людини може тривати на кілька десятків років, єдиною умовою залишається довічний прийом відповідних лікарських препаратів.
Підступністю вірусу імунодефіциту людини також є його мутування. Так, якщо лікарські препарати проти ВІЛ не змінити через деякий час, що визначається, виходячи з постійного контролю за хворобою, вірус пристосовується, і призначена схема лікування стає неефективною. Тому, з різною періодичністю, лікар змінює схему лікування, а разом із нею і ліки. Причиною зміни препарату також може бути його індивідуальна непереносимість пацієнтом.
Сучасна розробка ліків націлена не тільки на досягнення мети ефективності проти ВІЛ, але й на зменшення побічних ефектів від них.
Ефективність лікування також підвищується при зміні способу життя людини, покращення її якості – здоровий сон, правильне харчування, уникнення стресів, активний спосіб життя, позитивні емоції тощо.
Таким чином, можна виділити такі пункти у лікуванні ВІЛ-інфекції:
- Медикаментозне лікування ВІЛ-інфекції;
- Дієта;
- Профілактичні заходи.
Важливо!Перед застосуванням лікарських препаратів обов'язково зверніться до лікаря за консультацією!
1. Медикаментозне лікування ВІЛ-інфекції
На початку потрібно відразу ще раз нагадати, що СНІД є останньою стадією розвитку ВІЛ-інфекції, і саме на цій стадії у людини зазвичай залишається зовсім небагато часу для життя. Тому дуже важливо не допустити розвитку СНІДу, і багато в чому це залежить від своєчасної діагностики та адекватної терапії ВІЛ-інфекції. Також ми зазначили, що єдиним методом лікування ВІЛ сьогодні вважається високоактивна антиретровірусна терапія, яка за статистикою знижує ризик формування СНІД практично до 1-2 %.
Високоактивна антиретровірусна терапія (ВААРТ)– метод лікування ВІЛ-інфекції, що базується на одночасному прийомі трьох або чотирьох препаратів (тритерапія). Кількість препаратів пов'язана з мутагенності вірусу, і щоб пов'язувати його на цьому етапі максимально довго, лікар підбирає саме комплекс ліків. Кожен із препаратів, залежно від принципу дії, входить в окрему групу – інгібітори зворотної транскриптази (нуклеозидні та ненуклеозидні), інгібітори інтегрази, інгібітори протеази, інгібітори рецепторів та інгібітори фузії (інгібітори злиття).
ВААРТ має такі цілі:
- Вірусологічна – спрямована на усунення розмноження та розповсюдження ВІЛ, показником чого є зниження вірусного навантаження в 10 і більше разів за 30 днів, до 20-50 копій/мл і менше за 16-24 тижнів, а також утримання цих показників якомога довше;
- Імунологічна – спрямована на відновлення нормального функціонування та здоров'я імунної системи, що обумовлено відновленням кількості CD4-лімфоцитів та адекватною імунною відповіддю на інфекцію;
- Клінічна – спрямована на недопущення формування вторинних інфекційних захворювань та СНІД, що дає можливість зачати дитину.
Ліки від ВІЛ-інфекції
Нуклеозидні інгібітори зворотної транскриптази- Механізм дії заснований на конкурентному придушенні ферменту ВІЛ, що забезпечує створення ДНК, в основі якої лежить вірус РНК. Є першою групою препаратів проти ретровірусу. Переносяться досить добре. Серед побічних ефектів можна виділити – лактацидоз, пригнічення кісткового мозку, полінейропатію та ліпоатрофію. Речовина виводиться з організму у вигляді нирок.
Серед нуклеозидних інгібіторів зворотної транскриптази можна виділити - абакавір («Зіаген»), зидовудин («Азідотімідін», «Зідовірин», «Ретровір», «Тімазид»), ламівудін («Віролам», «Гептавір-150» », «Епівір»), ставудін («Актастав», «Зерит», «Ставудін»), тенофовір («Віреад», «Тенвір»), фосфазид («Нікавір»), емтрицитабін («Емтріва»), а також комплекси абакавір+ламівудін («Ківекса», «Епзіком»), зидовудин+ламівудін («Комбівір»), тенофовір+емтрицитабін («Трувада») та зидовудин+ламівудін+абакавір («Тризивір»).
Ненуклеозидні інгібітори зворотної транскриптази– делавірдін («Рескриптор»), невірапін («Вірамун»), рілпівірін («Едюрант»), ефавіренз («Регаст», «Сустіва»), етравірин («Інтеленс»).
Інгібітори інтегразимеханізм дії заснований на блокуванні ферменту вірусу, який бере участь в інтеграції вірусної ДНК в геном клітини-мішені, після чого утворюється провірус.
Серед інгібіторів інтегрази можна виділити – долутегравір («Тівікай»), ралтегравір («Ісентресс»), елвітегравір («Вітекта»).
Інгібітори протеази- Механізм дії заснований на блокуванні ферменту протеази вірусу (ретропепсин), який бере участь безпосередньо в розщепленні поліпротеїнів Gag-Pol на окремі білки, після чого власне і утворюються зрілі білки віріона вірусу імунодефіциту людини.
Серед інгібіторів протеази можна виділити – ампренавір («Агенераза»), даранавір («Презиста»), індинавір («Криксиван»), нелфінавір («Вірасепт»), ритонавір («Норвір», «Рітонавір»), саквінавір Інвіраза»), типранавір («Аптівус»), фосампренавір («Лексива», «Телзір»), а також комбінований засіб лопінавір + ритонавір («Калетра»).
Інгібітори рецепторів- Механізм дії заснований на блокуванні проникнення ВІЛ у клітину-мішень, що обумовлено впливом речовини на корецептори CXCR4 та CCR5.
Серед інгібіторів рецепторів можна виділити маравірок («Целзентрі»).
Інгібітори фузії (інгібітори злиття)- Механізм дії заснований на блокуванні останнього етапу щодо впровадження вірусу в клітину-мішень.
Серед інгібіторів злиття можна виділити енфувіртид (Фузеон).
Застосування Ваарт при вагітності знижує ризик передачі інфекції від інфікованої матері до дитини до 1%, хоча без цієї терапії відсоток зараження дитини становить близько 20%.
Серед побічних ефектів від застосування лікарських препаратів ВААРТ можна виділити панкреатит, анемії, шкірні висипання, камені в нирках, периферична нейропатія, лактатацидоз, гіперліпідемія, ліподистрофія, а також синдром Фанконі, синдром Стівенса-Джонсона та інші.
 Дієта при ВІЛ-інфекції спрямована на недопущення втрати ваги хворого, а також забезпечення клітин організму необхідною енергією і, звичайно, стимулювання та підтримання нормального функціонування не лише імунної, а й інших систем.
Дієта при ВІЛ-інфекції спрямована на недопущення втрати ваги хворого, а також забезпечення клітин організму необхідною енергією і, звичайно, стимулювання та підтримання нормального функціонування не лише імунної, а й інших систем.
Також необхідно звернути увагу на певну вразливість ослабленого інфекцією імунітету, тому зберігати себе від інфікування іншими видами інфекції — обов'язково дотримуйтесь правил особистої гігієни та правил приготування страв.
Харчування при ВІЛ/СНІД має:
2. Бути висококалорійним, через що в їжу рекомендується додавати олію, майонез, сир, сметану.
3. Включати багато пиття, особливо корисно пити відвари і свіжі соки з великою кількістю вітаміну С, який стимулює роботу імунітету - відвар, соки (яблучний, виноградний, вишневий).
4. Бути частим, 5-6 разів на добу, але невеликими порціями.
5. Води для пиття та приготування їжі повинні бути очищеними. Уникайте вживання прострочених продуктів, недовареного м'яса, сирих яєць, пастеризованого молока.
Що можна їсти при ВІЛ-інфекції:
- Супи – овочеві, на крупах, з вермішелью, на м'ясному бульйоні, можна з додаванням вершкового масла;
- М'ясо - яловичина, індичка, курка, легені, печінка, нежирні види риби (бажано морський);
- Крупи - гречана, перлова, рисова, пшоняна і вівсяна;
- Каші - з додаванням сухофруктів, меду, варення;
- Хліб;
- Жири – соняшникова мало, вершкове масло, маргарин;
- Рослинна їжа (овочі, фрукти, ягоди) – морква, картопля, капуста, кабачки, гарбуз, бобові, горошок, яблука, виноград, сливи та інші;
- Солодке - мед, варення, повидло, джем, мармелад, пастила, цукор, солодка випічка (не частіше ніж 1 раз на місяць).
Також при ВІЛ-інфекції та СНІД спостерігається дефіцит таких і
3. Профілактичні заходи
Профілактичні заходи при ВІЛ-інфекції, яких необхідно дотримуватись при лікуванні включають:
- Уникнення повторного контакту з інфекцією;
- Здоровий сон;
- Дотримання правил особистої гігієни;
- Уникнення можливості інфікування іншими видами інфекції - та інші;
- Уникнення стресів;
- Своєчасне вологе прибирання у місці проживання;
- Відмова від тривалого перебування під сонячним промінням;
- Повна відмова від алкогольної продукції, куріння;
- Повноцінне харчування;
- Активний спосіб життя;
- Відпочинок на морі, горах, тобто. у максимально екологічно чистих місцях.
Додаткові заходи щодо профілактики ВІЛ ми розглянемо наприкінці статті.
 Важливо!
Перед застосуванням народних засобів проти ВІЛ-інфекції обов'язково проконсультуйтеся з лікарем!
Важливо!
Перед застосуванням народних засобів проти ВІЛ-інфекції обов'язково проконсультуйтеся з лікарем!
Звіробій.Насипте в емальовану каструлю добре висушену подрібнену траву і залийте її 1 л очищеної м'якої води, після поставте ємність на вогонь. Після того, як засіб закипить, варіть засіб ще протягом 1 години на повільному вогні, потім зніміть, остудіть, процідіть і перелийте відвар у банку. Додайте у відвар 50 г олії обліпихи, ретельно перемішайте і відставте в холодне місце для настоювання, на 2 доби. Приймати засіб потрібно по 50 г 3-4 рази на день.
Солодка.Всипте в емальовану каструлю 50 г подрібненого, залийте її 1 л очищеної води і поставте на плиту на великий вогонь. Довівши до кипіння, зменшіть вогонь на мінімальне значення та протоміть засіб ще близько 1 години. Після цього зніміть відвар з плити, остудіть його, процідіть, перелийте в скляну тару, додайте сюди ж 3 ст. ложки натурального, перемішайте. Пити відвар потрібно по 1 склянці вранці, натще.
Прополіс.Залийте 10 г подрібненої половиною склянки води та поставте засіб на водяну баню, для томлення протягом 1 години. Після цього остудіть засіб і приймайте його 1-3 рази на день, по 50 г.
Сироп з ягід, яблук та горіха.Змішайте між собою в емальованій каструлі 500 г свіжих ягід червоної, 500 г брусниці, 1 кг нарізаних яблук зелених сортів, 2 склянки подрібнених, 2 кг цукру та 300 мл очищеної води. Відставте на час, поки цукру не розчиниться, потім поставте засіб на маленький вогонь, на 30 хвилин і зваріть сироп. Після сироп необхідно остудити, перелити в банку і приймати вранці, натще, по 1 ст. ложці, яку можна запитати ковтком кип'яченої води.
 Профілактика ВІЛ включає:
Профілактика ВІЛ включає:
- Дотримання;
- Обстеження донорів крові та органів;
- Обстеження всіх вагітних на наявність антитіл до ВІЛ;
- Контроль за народженням дітей у ВІЛ-позитивних жінок та попередження від грудного вигодовування;
- Проведення уроків щодо інформування молоді про наслідки деяких статевих відносин;
- Існують рухи по роботі з наркоманами, метою якого є психологічна допомога, навчення про безпечні ін'єкції та обмін голок та шприців;
- Зниження масштабів наркоманії та проституції;
- Відкриття центрів реабілітації наркозалежних людей;
- Пропагування безпечних статевих відносин;
- Відмова від неприродних статевих відносин (анальний, оральний секс);
- Дотримання медичними працівниками всіх правил безпеки роботи з біоматеріалами інфікованих людей, зокрема. такими захворюваннями, як;
- Якщо у медпрацівника стався контакт слизової або крові (поріз, прокол шкіри) з інфікованим біоматеріалом, рану необхідно обробити спиртом, після помити руки господарським милом і знову обробити спиртом, а також після цього в перші 3-4 години прийняти препарати з групи ВААРТ ( наприклад – «Азидотимідин»), що мінімізує можливість розвитку ВІЛ-інфекції та спостерігатися у інфекціоніста протягом 1 року;
- Обов'язкове лікування захворювань, що передаються статевим шляхом (ЗПСШ), щоб вони не перейшли у хронічну форму;
- Відмова від набивання татуювання, а також відвідування неперевірених салонів краси, косметологічних майстрів вдома, маловідомих стоматологічних клінік із сумнівною репутацією;
- Вакцина проти ВІЛ та СНІД станом на 2017 рік офіційно ще не розроблена, як мінімум, деякі препарати ще проходять доклінічні випробування.
 Такий вираз як «Люди, які живуть із ВІЛ» (ЛЖВ) використовується по відношенню до людини або групи осіб, які мають ВІЛ-позитивний статус. Цей термін вигадали у зв'язку з тим, що ЛЖВ можуть проживати в соціумі кілька десятків років, і піти з життя не від самої інфекції, а від природного старіння організму. ЛЖВ у жодному разі має бути клеймом, від якого треба цуратися і тримати в ізоляції. Також ЛЖВ мають такі самі права, як і ВІЛ-негативна людина – на медичну допомогу, освіту, роботу, народження дитини.
Такий вираз як «Люди, які живуть із ВІЛ» (ЛЖВ) використовується по відношенню до людини або групи осіб, які мають ВІЛ-позитивний статус. Цей термін вигадали у зв'язку з тим, що ЛЖВ можуть проживати в соціумі кілька десятків років, і піти з життя не від самої інфекції, а від природного старіння організму. ЛЖВ у жодному разі має бути клеймом, від якого треба цуратися і тримати в ізоляції. Також ЛЖВ мають такі самі права, як і ВІЛ-негативна людина – на медичну допомогу, освіту, роботу, народження дитини.
До якого лікаря звернутися за ВІЛ-інфекції?
ВІЛ-інфекція - відео